Impurezas elementares: o que são?
Impurezas elementares são metais pesados e suas diversas fontes de contaminação. Os fabricantes de medicamentos, assim, devem garantir que essas impurezas estejam dentro dos limites previamente estabelecidos (PDE) nos produtos fabricados, além de controlar as principais fontes de contaminação, visto que não oferecem nenhum benefício terapêutico para o paciente.
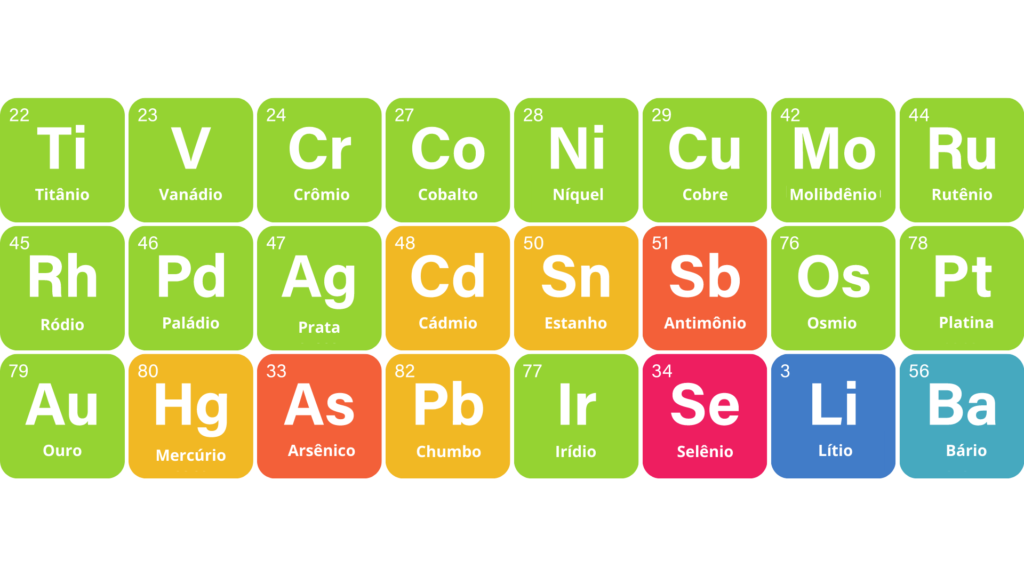
As impurezas são detectáveis no produto acabado e podem ser identificadas por meio do rastreamento de todos os passos do procedimento produtivo, identificando todos os componentes, materiais ou processos que possam contaminar o medicamento. Os elementos químicos que devem ser pesquisados individualmente são:
Essas impurezas são classificadas em 3 grupos de acordo com a sua toxicidade (PDE), pela probabilidade de uso no processo produtivo do medicamento e, ainda, pela quantidade presente nos materiais em contato com o produto (abundância do elemento).
Classe 1: impurezas de alta toxicidadespara os seres humanos, que tem utilidade limitada ou nula na fabricação de produtos farmacêuticos. Podem ser encontradas como impurezas de materiais comumente utilizados (por exemplo excipientes extraídos). Esses elementos devem ser pesquisados em todas as possíveis fontes de contaminação e incluídos na análise de risco do produto medicamentoso. As, Cd, Hg e Pb.
Classe 2:impurezas geralmente tóxicas para o ser humano, dependendo da via de administração. São divididas em duas subclasses com base em sua probabilidade relativa de ocorrência no medicamento:
- Classe 2A: probabilidade relativamente alta de ocorrência em medicamentos, exigindo, assim, análise de risco em todas as fontes potenciais de impurezas elementares, rota produtiva e vias de administração. Co, Ni e V.
- Classe 2B: probabilidade baixa de ocorrência em medicamentos, relacionada com a baixa abundância e baixo potencial de ser co-isolado com outros materiais. Por consequência, podem ser excluídos da análise de risco, a menos que sejam intencionalmente adicionados durante a fabricação de substâncias medicamentosas, excipientes ou outros componentes do medicamento. Ag, Au, Ir, Os, Pd, Pt, Rh, Ru, Se e Tl.
Classe 3:impureza com toxicidade relativamente baixa na administração por via oral, mas que requerem uma análise de risco se administrados por via inalatória ou parenteral. Ba, Cr, Cu, Li, Mo, Sb e Sn.
Existem algumas impurezas elementares para as quais a PDE ainda não foi estabelecida, devido às suas baixas toxicidade conhecidas, que mesmo assim podem comprometer funções importantes dos organismos (alumínio – funções renais, zinco e manganês – funções hepáticas). Se elas estiverem presentes em um medicamento, serão abordadas por outras diretrizes e/ou regulamentações regionais. Al, B, Ca, Fe, K, Mg, Mn, Na, W e Zn.
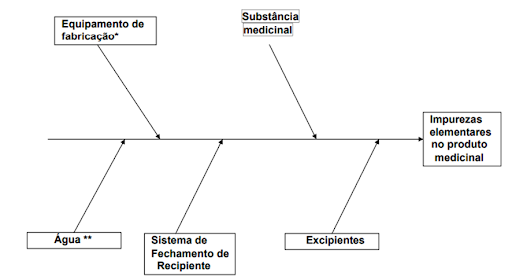
A diretriz ICH Q3D�sugere 5 potenciais fontes de impurezas em um medicamento acabado: água, processo de fabricação, sistema de fechamento de contêineres para embalagens, substância medicamentosa e excipientes inertes. Caso encontradas, devem constar na avaliação de risco outras fontes potenciais de contaminação. �
A pesquisa de impurezas elementares deve ser realizada por empresas farmacêuticas fabricantes dos seguintes tipos de medicamentos (comercializados e novos): sintéticos; medicamentos que contém proteínas e polipeptídeos (origens recombinantes e não recombinantes) e seus derivados; e, medicamentos que contém polipeptídeos, polinucleotídeos e oligossacarídeos sintéticos.
Já a pesquisa não se aplica aos seguintes tipos de medicamentos e terapias: fitoterápicos; radiofármacos; vacinas; células metabólicas; produtos provenientes de DNA; extratos alérgicos; células sanguíneas; componentes do sangue, incluindo o plasma e se seus derivados; soluções para diálise não utilizadas na circulação sistêmica; elementos intencionalmente incluídos no medicamento para fins terapêuticos (polivitamínicos contendo minerais); produtos para terapia genética; terapia celular; utilizados em terapias; e, medicamentos em fase de pesquisa clínica (estágio de desenvolvimento).
A pesquisa de impurezas elementares têm como finalidade a avaliação dos dados de toxicidade dos potenciais metais pesados (impurezas elementares); estabelecer o limite de exposição diária permitida (PDE) de cada elemento; identificar as fontes potenciais de contaminação; e, controlar o risco da presença de metais pesados nos medicamentos.
A InsilicAll dispõe de uma plataforma SaaS integrada à inteligência artificial, com tecnologia nacional exclusiva e proprietária. Por meio dessa ferramenta, é possível utilizar programas variados que, quando aplicados em conjunto, resultam em análises mais precisas e multifocais, acelerando o desenvolvimento da P&D, garantido pelas diferentes perspectivas exploradas.
Através de tecnologia própria, com um time de experts e uma a plataforma de drug discovery, realizamos controle de qualidade utilizando o aplicativo Detoxie®, que faz uso de big data e da inteligência artificial para acelerar a solução dos problemas relacionados ao risco toxicológico.
Na InsilicAll realizamos a análise de risco e a elaboração de relatório de acordo com as normas vigentes, incluindo avaliação de citotoxicidade e limite de exposição diária (PDE). Essa avaliação pode ser facilitada com informações sobre as impurezas elementares em potencial, providenciadas pelos fornecedores de substâncias medicinais, excipientes, sistemas de fechamento de recipientes e equipamentos de fabricação.
Acesse o artigo para saber mais sobre a plataforma SaaS e os demais aplicativos InsilicAll. Entre em contato conosco para mais informações, vantagens e orçamentos!�